-2차원 신소재 리본으로 오려낸다

[데일리비즈온 김소윤 기자] 국내 연구진이 기존에 보고된 바 없는 다원소로 구성된 물질을 리본 형태로 오려내는 신기술을 개발했다. 간단한 초음파 처리를 통해 절개하는 방식인데 기존 백금 촉매를 대체하면서 수소 반응 촉매가 될 것으로 보인다.
15일 한국과학기술원(KAIST)는 이 대학 신소재공학과 김상욱 교수 연구팀이 생명화학공학과 정유성 교수 연구팀과 공동연구로 2차원 반도체인 전이금속 칼코지나이드 물질을 얇은 리본 형태로 오려낼 수 있는 신기술을 개발했다고 밝혔다.
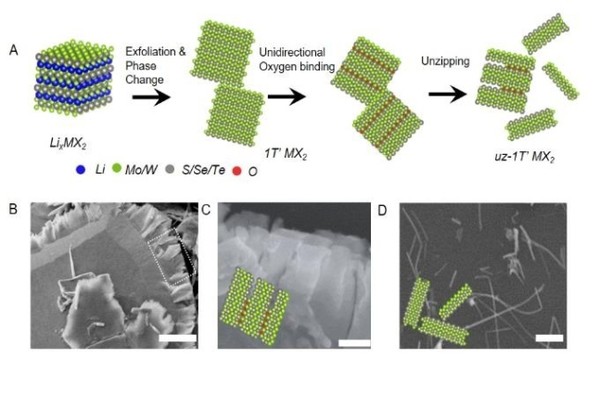
2차원 전이금속 칼코지나이드는 전이금속원소와 칼코겐 원소의 화합물이다. 평면 방향으로는 전이금속원소와 칼코겐 원소가 강한 공유결합을 하고 있다. 수직 방향으로 약한 반데르발스 결합을 하는 층상구조를 가지고 있기도 하다. 이를 이용해 층간 분리를 통해 2차원 단층 형태로 박리가 가능하다.
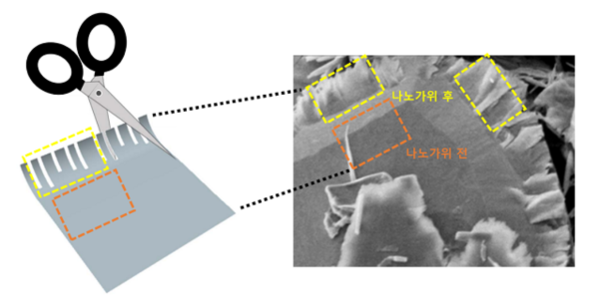
연구팀은 간단한 초음파 처리를 통해 2차원 전이금속 칼코지나이드 물질을 일정한 방향으로 절개해 긴 나노 리본 형태로 오려내는 데 세계 최초로 성공했다는 설명이다.
김상욱 교수와 정유성 교수 공동 연구팀이 개발한 이 신소재는 기존 백금 촉매를 대체하여 수소 발생 반응 촉매로 활용이 가능할 것으로 전망된다고 연구팀은 밝혔다.
◇ 세계 최초 ‘나노 가위’ 신기술
이에 따르면 수소는 공해물질을 배출하지 않기 때문에 기존의 화석연료를 대체할 수 있는 신 에너지 자원으로 주목받고 있다. 수소를 생산하는 가장 환경친화적인 방법은 화학적으로 물을 분해하는 방법인데 이 경우 효율적으로 수소를 생성할 수 있도록 값싸고 높은 효율의 촉매를 개발하는 것이 매우 중요하다는 설명이다.
2차원 전이금속 칼코지나이드 소재는 우수한 촉매 성능을 지니고 있어 에너지·환경 분야에 응용이 기대되는 소재다. 하지만 보다 높은 촉매 성능을 달성하기 위해서는 촉매 활성을 갖는 2차원 소재의 가장자리를 많이 노출하는 방법이 요구된다. 종이를 오려내듯 2차원 소재를 길쭉한 1차원 리본 형태로 오려내게 되면 더 많은 가장자리를 노출할 수 있기 때문이다.
현재까지는 그래핀과 같이 한가지 원소로만 이루어진 2차원 소재의 경우 여러 방법의 오려내는 기술이 알려졌지만 2개 이상의 원소로 이뤄진 2차원 전이금속 칼코지나이드 물질에 이를 적용하는 데 한계가 있는 실정이다.
이에 연구팀은 화학 반응을 통해 2차원 소재의 특성 변화를 유도한 후 저렴한 초음파 처리 공정을 통해 1차원 리본 형태로 오려내는 기술을 세계 최초로 개발해냈다. 이들은 2차원 소재 표면이 산소와 일정한 방향성을 가지고 화학 반응한다는 점을 발견하고 간단한 초음파 자극을 통해 1차원 리본 형태로 오려냈다.
이어 이 기술을 활용해 기존 고가의 백금 촉매에 견줄 만한 높은 성능을 지닌 수소 발생 반응 촉매를 구현할 수 있었다. 연구팀 관계자는 "기존에 보고된 적이 없는 다원소로 구성된 2차원 전이금속 칼코지나이드 소재를 오려내는 새로운 기술 개발을 계기로 다양한 다원소 저차원 나노 신물질을 제조할 것으로 크게 기대가 된다ˮ고 설명했다.
◇ 암 치료에도 활용되는 사례
나노 유전자 가위 관련 또 다른 기술은 암 치료에도 활용된 바 있다. 4월 아주대 윤태종 교수 연구팀과 가톨릭대 조영석 교수 연구팀이 나노-유전자 가위 기술을 활용해 대장암 치료제를 개발하기도 했다.
흔히 쓰이고 있는 대장암 항암제에 치료 효과를 보이지 않는 유전자 변이 대장암 환자들을 위한 치료법이라는 설명이다. 공동 연구팀은 나노 전달체에 유전자 가위 단백질 구조체를 탑재하는 방식을 통해 유전적 이상 부위를 효과적으로 편집하면서 기술을 개발해냈다.
세툭시맙 성분의 항암제는 대장암 치료를 위해 많이 쓰이고 있지만 암세포의 성장과 관련된 KRAS 유전자의 변이로 인해 치료 효과를 보지 못하는 환자가 많다는 점이 한계인 실정이었다. 대장암 환자 중 60% 정도는 약물에 저항을 나타내 치료 호전이 더뎠다.
많은 연구자들이 KRAS 유전자 변이에 의한 암을 치료하기 위해 시도했지만 유전자 변이로 인해 지속적으로 암이 재발했다. 이에 근본적 치유 방법에 대한 연구가 요구됐다. 이에 유전자 가위 기술을 활용하는 것이 대안으로 떠올랐는데 단백질 형태의 유전자 가위 소재가 체내에서 안정성이 크게 저하되어 효율성 문제의 해결이 어려웠다.
연구팀은 이에 나노 전달체에 유전자 가위 단백질 구조체를 탑재하여 유전적 이상 부위를 효과적으로 편집했고 높은 치료 효과를 보일 수 있음을 밝혀냈다. 연구팀은 나노 리포좀 구조체를 사용하여 KRAS 유전자 변이 부위를 편집할 수 있는 유전자 가위 단백질 소재를 더했다.

