-항암제 효능 높일 수 있는 기술 개발
-항암제 표적을 이용해 역발상 연구

[데일리비즈온 김소윤 기자] 국내 연구진이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다. 앞으로 항암제를 이용한 암 치료에 새로운 길이 열렸다.
24일 한국과학기술원(KAIST)는 이 대학 바이오및뇌공학과와 생명과학과 공동연구팀이 항암제의 표적 단백질을 전달체로 이용하는 역발상 연구결과를 내놨다고 밝혔다. 이번 연구에는 김진주·이준철 박사과정 학생이 공동 제1 저자, 전상용·최명철 교수가 공동 교신저자로 참여했다.
◇ 암 치료 위한 나노 튜브 전달체 개발
이에 따르면 몸속 세포가 분열할 때 염색체들은 세포 한가운데에 정렬해 두 개의 딸세포로 나뉜다. 이 염색체들을 끌어당기는 끈이 ‘미세소관’이다. 이는 ‘튜불린’ 단백질로 이루어진 긴 튜브 형태의 나노 구조물이다.
미세소관을 표적으로 하는 항암 약물인 ‘미세소관 표적 치료제’는 임상에서 다양한 암의 치료에 활용되고 있다. 암세포 미세소관에 결합해 끈 역할을 방해한다. 암세포의 분열을 억제, 결국 사멸을 유도하는 원리다.
튜불린 단백질에는 이 약물이 강하게 결합하는 고유의 결합 자리가 있다. 이에 착안한 연구진은 표적 물질(튜불린 단백질)을 약물 전달체로 사용한다는 아이디어를 발상했는데 이는 세계 최초다.
연구팀은 튜불린 나노 튜브의 약자를 딴 TNT로 이름 붙인 전달체를 개발했다. 이 전달체를 이용해 항암 효능을 확인할 수 있었다. TNT라는 명칭엔 암 치료를 위한 폭발물이라는 뜻도 담겼다.
TNT에 자발적으로 탑재되는 미세소관 표적 치료제는 각 항암제마다 맞는 전달체를 찾아야 하는 기존의 한계를 해결해준다. TNT는 미세소관을 표적으로 하는 모든 약물을 탑재할 수 있는 전달체이기 때문이다.
◇ TNT는 미세소관 표적으로 하는 만능 전달체
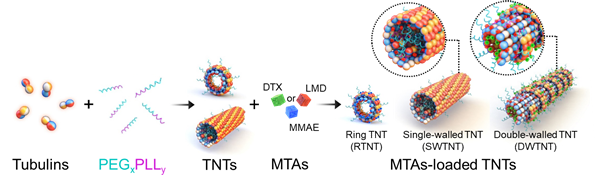
우선 연구팀은 튜불린 단백질에 블록 혼성 중합체(PEG-PLL)를 섞어 TNT 구조를 만들었다. 튜불린은 빌딩 블록을 뜻하고 PEG-PLL은 이것들을 붙여주는 접착제를 말한다. 이 다음 도세탁셀, 라우리말라이드, 모노메틸아우리스타틴 E 3종의 약물이 TNT에 탑재됨을 보였다. 해당 약물들은 실제 유방암, 두경부암 등의 화학요법에 활용되고 있는 약제다.
아울러 연구팀은 탑재되는 약물의 종류와 개수에 따라 TNT의 구조가 변할 뿐 아니라 약물 전달체로서의 물리·화학적 특성도 달라진다는 것을 알아냈다. TNT가 탑재하려는 약물에 맞춰 자발적으로 형태를 변형하는 ‘적응형 전달체’라는 것이다.
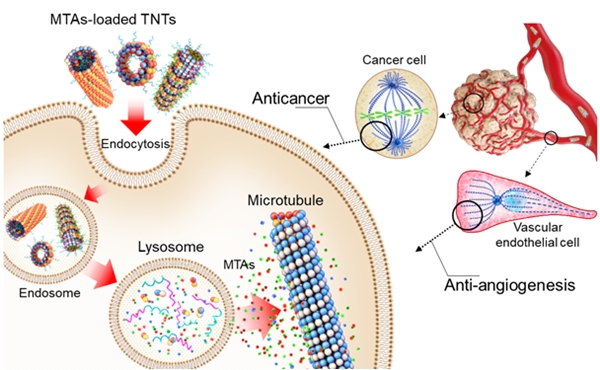
이들은 항암제가 탑재된 TNT가 엔도좀-리소좀 경로로 암세포에 들어가 뛰어난 항암 및 혈관 형성 억제 효과를 보이는 것도 확인했다. 이는 세포 및 동물을 대상으로 한 실험을 통해 밝혀낼 수 있었다.
이러한 약물 전달체가 성공적으로 구현할 수 있던 이유는 연구진이 보유한 튜불린 분자 제어 기술력이 있었기 때문이다. 연구진은 튜불린 단백질을 레고 블록으로 여겼는데 이 형태를 변형하기도 하고 블록처럼 쌓는 방식을 제어해 조립하는 등의 노하우를 보유했다.
연구팀 관계자는 “이번 연구결과는 지금까지 학계에 보고되지 않은 완전히 새로운 방식의 약물 전달체를 구현했다는 점에서 의미가 크다”며 “TNT는 개발예정인 미세소관 표적 치료제까지 운송할 수 있는 범용적인 전달체이며 다양한 항암제들의 시너지 효과를 기대할 수 있는 ‘플랫폼 전달체’가 될 것”이라고 말했다.
◇ 튜불린 단백질을 레고 블록처럼 변형
앞서 한 병원에서는 표적 항암제의 환자 반응범위를 넓힐 실마리를 찾기도 했다. 18일 삼성서울병원은 박웅양 유전체연구소장과 사빈 테파 벨기에 루벤대 교수팀이 이러한 연구결과를 내놨다고 밝혔다.
전이성 대장암은 수술 치료가 어렵다. 최근 암세포만 선택적으로 공격하는 표적 항암제를 통한 치료가 시도되고 있다. 전이성 대장암 환자의 생존 기간을 최대 5배까지 늘릴 수 있는 치료법이지만 환자의 약 15%만 해당 표적 항암제에 반응한다는 한계가 있었다.
연구팀은 국내 대장암 환자 23명과 벨기에 환자 6명의 암 조직을 개별 세포 단위로 분리했다. 91103개의 단일 세포로 분리한 뒤 하나씩 유전체 정보를 분석한 연구팀은 이 과정을 통해 암의 성장과 전이 과정에 영향을 미치는 암의 미세환경을 알아봤다.
이 결과 대장암 조직 내 근섬유아세포와 골수성 세포가 면역 억제 기능을 햇다. 근섬유아세포는 상처가 위축되는 데 관여하는 세포로 수축하는 특징이 있다. 골수성 세포는 골수를 이루는 줄기세포다.
연구팀 관계자는 “이 세포들이 ‘형질전환증식인자(TGF-β)’의 과다발현을 유도했다”며 “TGF-β는 암 세포를 면역세포로 보호하는 기능이 있어 면역항암제 치료 효과를 낮춘다”고 설명했다.

